2025年5月,公共卫生学院赵杨教授课题组在国际权威期刊《自然·通讯》(Nature Communications)发表题为《全基因组交叉性状分析表征肺部和胃肠道疾病之间的共同遗传结构》(A genome-wide cross-trait analysis characterizes the shared genetic architecture between lung and gastrointestinal diseases)的研究论文。该研究基于大规模的全基因组关联研究(GWAS)数据,系统解析了肺部与胃肠道疾病共病的遗传机制,识别出多效性遗传位点(SNP)、关键基因及相关生物学通路,为理解“肠-肺轴(gut-lung axis, GLA)”提供了多组学证据。

肺部与胃肠道疾病常呈共病状态,显著影响患者健康结局。近年来,GLA概念的提出强调了肠道菌群、免疫细胞及炎症因子在两类疾病互作中的关键作用。尽管已有研究证实环境因素(如吸烟)可通过GLA影响疾病风险,但关于其遗传机制的系统性研究仍属空白。
研究整合了欧洲(EUR)、东亚(EAS)及非洲(AFR)人群的肺部与胃肠道疾病的GWAS数据,在EUR人群中识别出27对具有显著遗传相关性的疾病组合。通过交叉性状Meta分析、精细定位及共定位分析,研究共鉴定出42个候选多效性SNP,其中5个SNP在多个疾病对中共享,另发现3个新的全基因组显著多效性SNP,包括可能调控基因表达的rs55673000。
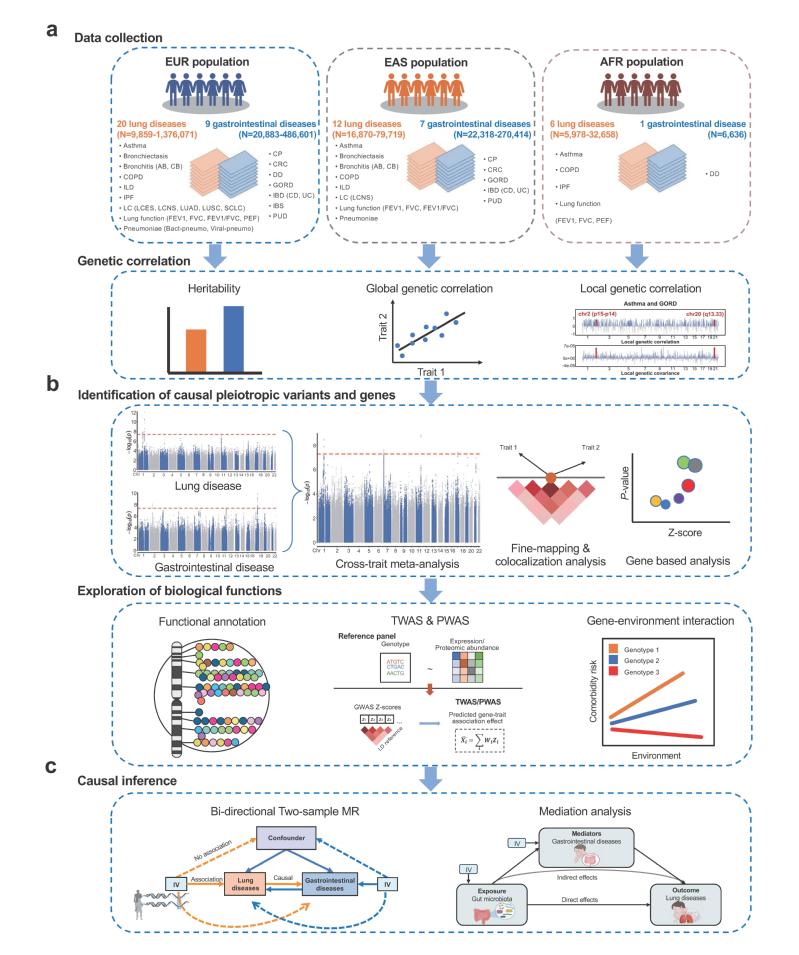
在功能注释方面,研究结合GSEA、TSEA、CSEA、TWAS及PWAS等多组学方法,在42个候选多效性SNP对应的14对肺-胃肠道疾病对子中,平均识别出112个风险基因,并筛选出66个候选多效性基因,主要富集于免疫与炎症相关通路。TWAS与PWAS进一步验证了基因表达与蛋白水平在疾病共病中的作用。
此外,研究还评估了42个候选多效性SNP与可改变暴露因素之间的交互作用,发现如BMI、吸烟、空气污染及心理健康状况等平均50种暴露因素与共病险相关。其中,rs2754246与不良心理健康状况在哮喘(asthma)-胃食管反流(GORD)之间的交互作用尤为显著。
通过双向孟德尔随机化分析,研究确认了asthma与GORD等4对性状之间的显著因果关联。进一步结合肠道微生物的汇总数据进行中介分析,揭示了Parasutterella-GORD-asthma(中介比例38.78%)及Faecalibacterium-GORD-慢性支气管炎(中介比例28.63%)两条潜在疾病通路,为肺-胃肠共病的微生态机制提供了新视角。
本研究首次在全基因组层面系统刻画了肺部与胃肠道疾病的共享遗传结构,识别出一系列未表征的多效性遗传标志物,为相关疾病的机制研究与干预策略开发提供了重要理论依据。
我校公共卫生学院赵杨教授与靳光付教授为共同通讯作者,尤东方副教授、吴雅倩博士、陆梦依讲师为本文的共同第一作者。
原文链接:https://doi.org/10.1038/s41467-025-58248-w
