2024年3月20日,我院钱旭教授与基础医学院汪秀星教授以及南京医科大学第一附属医院尤永平教授团队在Science Translational Medicine杂志发表了题为:Reactivating PTEN to impair glioma stem cells by inhibiting cytosolic iron-sulfur assembly pathway的研究论文,揭示了促癌代谢物延胡索酸(fumarate)介导的PTEN琥珀酸化修饰在促胶质瘤干细胞(GSCs)干性维持及放化疗抵抗中的关键作用,并基于此机制提出PTEN重激活干预措施。

GSCs是肿瘤组织中具有自我更新、多向分化、无限增殖能力的一类细胞,对胶质瘤的生长、浸润及放化疗抵抗有重要作用。相较于分化的胶质瘤细胞,GSCs的DNA损伤修复能力更强,对放化疗具有更高的耐受性。抑癌基因PTEN失活突变是胶质瘤,尤其是胶质母细胞瘤(GBM)最常发生的遗传学事件之一。约60-70%的 GBM患者肿瘤组织发生PTEN功能失活。钱旭教授课题组围绕肿瘤代谢开展了系列研究,前期研究发现在PTEN活性缺失的胶质瘤病人组织中,PGK1自磷酸化水平升高,并且与病人不良预后密切相关(Molecular Cell, 2019)。然而剩余的20-30%患者即使是PTEN野生型却仍然能够发展成胶质母细胞瘤。野生型PTEN如何在GBM特别是GSCs中功能失活、以及如何重激活PTEN抑癌作用值得深入探讨。
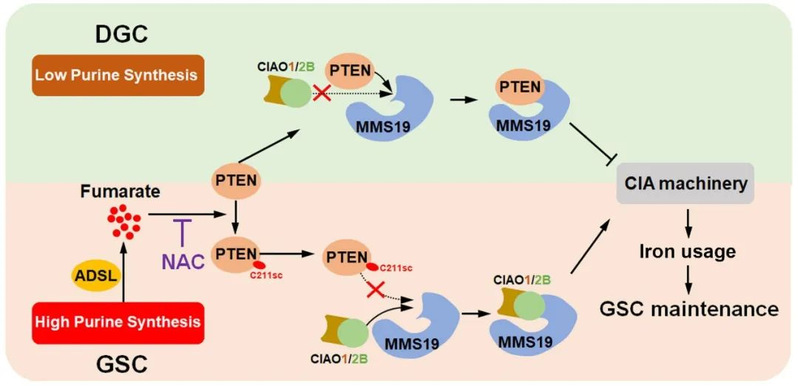
该研究发现,在分化肿瘤细胞中,PTEN通过与CIAO2B竞争性结合MMS19,抑制细胞质铁硫簇组装(CIA),阻碍铁元素利用,从而抑制肿瘤恶性表型。课题组前期发现Fumarate可以通过半胱氨酸琥珀酸化修饰PTEN,抑制PTEN膜定位促进PI3K/AKT信号通路激活(Molecular Cell, 2022)。在本研究中,该团队进一步发现在GSCs中,高嘌呤合成代谢导致副产物fumarate水平显著增高,介导PTEN的C211位点发生琥珀酸化修饰。C211位点琥珀酸化修饰可抑制PTEN与MMS19的结合,从而促进铁元素利用和DNA代谢稳态,最终导致GSCs放化疗抵抗。靶向嘌呤代谢中产生fumarate的关键酶ADSL可显著减少细胞中fumarate水平,增加肿瘤细胞放化疗敏感性。
最后,研究团队探索了靶向fumarate提高胶质瘤治疗敏感性的临床转化潜能。基于“以彼之道还施彼身”的思路,研究人员通过外源性给予肿瘤细胞大量半胱氨酸消耗细胞中fumarate。乙酰半胱氨酸(NAC)是一款经典祛痰药,目前广泛应用于呼吸道疾病治疗。NAC进入细胞后,其携带的自由巯基可与fumarate发生迈克尔加成反应,消耗细胞中fumarate。研究结果表明,联合使用NAC可大大增加GSCs治疗敏感性。该研究成果对于推动NAC “老药新用”,增加胶质瘤患者的临床治疗手段具有重要指导意义。
我院钱旭教授、南京医科大学第一附属医院神经外科尤永平教授与基础医学院汪秀星教授为该论文共同通讯作者。南京医科大学姑苏学院博士后尹建星、南京医科大学公共卫生学院葛新副教授和南京医科大学公共卫生学院博士生丁方舒为该论文共同第一作者。
原文链接:https://www.science.org/doi/10.1126/scitranslmed.adg5553
